Se le denomina gases al estado de agregación de la materia en el cual , bajo ciertas condiciones de temperaturas y presión , sus moléculas interaccionan débilmente entre si , sin formar enlaces moleculares , adoptando la forma y el volumen del recipiente que las contiene y tendiendo a separarse, esto es, expandirse, todo lo posible por su alta energía cinética
Volumen
Temperatura
Presión
n = moles Ps/mm
Temperatura: Vibración de las moléculas o átomos en sistemas - se mide con termómetro
Calor: Energía propia de un sistema calórico - colorímetro
Ejemplo:
Convertir de Kelvin a Celsius
* 284°K a °C
284°K - 273°K = 11°C
Convertir de Celsius a Kelvin
* 80°C a °K
80°C + 273°K = 353°K
TEORIA CINETICA MOLECULAR
La teoría cinética de los gases es una teoría física y química que explica el comportamiento y propiedades macroscópicas de los gases, a partir de una descripción estadística de los procesos moleculares microscópicos. La teoría cinética se desarrolló con vase en los estudios de físicos como Daniel Bernoulli en el siglo XVIII, Ludwing Boltzmann y James Clerk Maxwell a finales del siglo XIX.
Características:
- A mayor volumen, mayor presión.
- Se expanden las moléculas y se chocan con la presión.
- El volumen y la presión se comprimen.
Ley de BOYLE
La presión ejercida por una fuerza química es inversamente proporcional a la masa gaseosa, siempre y cuando su temperatura se mantenga constante (si el volumen aumenta la presión disminuye, y si la presión aumenta el volumen disminuye.
Un sistema inicial registra las siguientes características, tiene un orden inicial de 500ml y un volumen final de 300ml
¿Cuál es la presión inicial?
P1 = 1,2 Atm V1 = 500ml P2 = 2Atm V2 = 300ml
P1 = P2 * V2 / V1
P1 = 2Atm * 0,3L / 0,5L
P1 = 0,6 / 0,5
P1 = 1,2Atm
Ley de CHARLES
Una cierta cantidad de gas a una presión constante, al aumentar la temperatura, el volumen del gas aumenta y al disminuir la temperatura, el volumen del gas disminuye. Esto se debe a que la temperatura está directamente relacionada con la energía cinética debido al movimiento de las moléculas del gas. Así que, para cierta cantidad de gas a una presión dada, a mayor velocidad de las moléculas (temperatura), mayor volumen del gas.
Ejemplo:
Calcular el volumen final de un sistema que registra las siguientes conclusiones iniciales, temperatura 50°
T1 = 50°C 323°K T2 = 100°C 373°K
V1 = 400ml 0,4L V2 = 460ml
V2 = 0,4L * 373°K / 323°K
V2 = 149,2L / 323
V2 = 0,46L = 460ml
Ley de GAY LUSSAC
La ley de Gay- Lussac establece la relación entre la temperatura y la presión de un gas cuando el volumen es constante.
Al aumentar la temperatura las moléculas del gas se mueven más rápidamente y por tanto aumenta el número de choques contra las paredes, es decir aumenta la presión ya que el recipiente es de paredes fijas y su volumen no puede cambiar.
Ejemplo:
Un gas registra las siguientes condiciones se conoce su temperatura inicial que es 200°k y así mismo el gas posee condiciones tiene una presión final de 2 Atm y una temperatura de 0°C
calcular la presión inicial
P1= P2 * T1 / T2
P1= 2Atm * 200°K / 273°K
P1= 200 / 273
P2= 1,46 Atm
Ley COMBINADA DE GASES
La ley general de los gases o ley combinada dice que una masa de un gas ocupa un volumen que está determinado por la presión y la temperatura de dicho gas. Estudia el comportamiento de una determinada masa de gas si ninguna de esas magnitudes permanece constante.
V * P2 / T1 = V2 * P2 / T2
VIPITO = VOPOTI
Vi * Pi * T2 = V2* P2 * T1
V1* P1 * T2 / V2* P2 = V2
V1 = V2 * P2 * T1 / P1 * T2
V2 = V1 * P1 * T2 / P2 * T1
P1 = V2 * P2 * T1
P2 = V1 * P1 * T2 / V2* T1
T1 = V1* P1 * T2 / T1* P2
T2 = V2 * P2 * T1 / V1 * P1
Ejemplo:
Se tiene un gas a un volumen que ocupara un gas en el cual tienen un volumen inicial de 500ml , una presión inicial de 2 Atm a una temperatura inicial de 3°C y las condiciones finales de las siguiente 3 s Atm a una temperatura de 10°C
Calcular el volumen final
V1 = 500ML P1= 2 Atm T1= 3°C + 273 = 276°K P2 = 3,5 Atm
T2 = 10°C + 273°K = 283°K V2 = 0,29 L
V2 = V1 * P1 * T2 / P2 * T1
V2 = 283 / 966
V2 = 0,29L
La química orgánica es la disciplina científica que estudia la estructura,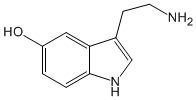 Serotoninapropiedades, síntesis y reactividad de compuestos químicos formados principalmente por carbono e hidrógeno, los cuales pueden contener otros elementos, generalmente en pequeña cantidad como oxígeno, azufre, nitrógeno, halógenos, fósforo, silicio.
Serotoninapropiedades, síntesis y reactividad de compuestos químicos formados principalmente por carbono e hidrógeno, los cuales pueden contener otros elementos, generalmente en pequeña cantidad como oxígeno, azufre, nitrógeno, halógenos, fósforo, silicio.
 Serotoninapropiedades, síntesis y reactividad de compuestos químicos formados principalmente por carbono e hidrógeno, los cuales pueden contener otros elementos, generalmente en pequeña cantidad como oxígeno, azufre, nitrógeno, halógenos, fósforo, silicio.
Serotoninapropiedades, síntesis y reactividad de compuestos químicos formados principalmente por carbono e hidrógeno, los cuales pueden contener otros elementos, generalmente en pequeña cantidad como oxígeno, azufre, nitrógeno, halógenos, fósforo, silicio.
LABORATORIO " IDENTIFICACION DE CARBOHIDRATOS"










En este laboratorio pudimos observar cuando un alimento contiene carbohidratos.
MATERIALES
- Recipiente para colocar el alimento
- Papa francesa
- Yuca
- Tintura de yodo
- Salchicha
- Chito
- Papas fritas
- Carne
- Pan
- Papa
- Pollo
PROCEDIMIENTO
- Colocamos cada alimento en un recipiente llano
- Utilizamos dos gotas con cada alimento , obteniendo así un color negro sobre todos estos.
- Por ultimo nuestro objetivo fue verificar que cada uno de ellos fuera carbano , pero la carne no es carbono por lo tanto no tuvo ningun color y reaccion ante la tintura de yodo.
RESULTADOS










CONCLUSIÓN
En conclusión nuestro proceso fue de mucho aprendizaje ya que pudimos diferenciar los alimentos que poseen carbohidratos y los que que no , en este caso el que mas posee cabohidratos es el pan, lo clasificamos así ya que su colo fue el mas concentrado notandose un color oscuro e intenso.
LABORATORIO " ESTRUCTURA DE ALCANOS , ALQUENOS Y ALQUINOS"
En este laboratorio realizamos la estructura de los alcanos , alquenos y alquinos , con sus respectivos átomos de carbono e hidrógeno.
ALCANOS:
Los alcanos son hidrocarburos, es decir que tienen sólo átomos de carbono e hidrógeno. La fórmula general para alcanos alifáticos (de cadena lineal) es CnH2n+2, y para cicloalcanos es CnH2n. También reciben el nombre de hidrocarburos saturados de cadena abierta que tiene enlaces sencillos: carbono-carbono y carbono-hidrogeno.









ALQUENOS:
Los alquenos son compuestos insaturados que contienen en su estructura cuando menos un doble enlace carbono-carbono. Fórmula general: CnH2nPor lo tanto, los alquenos si sustituyen tres tienen el doble de hidrógenos que carbonos. La terminación sistémica de los alquenos es ENO. El más sencillo de los alquenos es el eteno, conocido más ampliamente como etileno, su nombre común. La mayor parte de los alquenos se obtienen del petróleo crudo y mediante la deshidrogenación de los alcanos.









ALQUINOS:
Los alquinos son hidrocarburos insaturados que contienen en su estructura cuando menos un triple enlace carbono-carbono. Fórmula general: CnH2n-2. La terminación sistémica de los alquinos es INO. El más sencillo de los alquinos tiene dos carbonos y su nombre común es acetileno, su nombre sistémico etino.









MATERIALES:
- Bolas de icopor Medianas y pequeñas
- Palitos pincho
- Palillos pequeños
- Adhesivos
PROCEDIMIENTO
- Tomamos las bolitas de icopor y las unimos junto con los palos de pincho y los palillos mas pequeños
- Escribimos , recortamos y pegamos los adhesivos sobre cada estructura de alcanos , alquenos y alquinos.
- Agregamos la cantidad de pallios y bolitas segun la numeracion de cada uno.
CONCLUSIÓN
Podemos decir que fue un trabajo de mucha habilidad y rapidez , donde aprendimos a diferenciar claramente los alcanos , alquenos y alquinos. Debemos tener en cuenta lo que compone su estructura.
En este laboratorio optamos por realizar el proceso de destilacion de alcoholes por arrastre de vapor donde pudimos observar que consiste en un proceso de calentar un liquido hasta que llegue a su condensacion y asi libere ciertos componentes que hace que este sea mas contaminante.
MARCO TEORICO
La destilación por arrastre con vapor es una técnica usada para separar sustancias orgánicas insolubles en agua y ligeramente volátiles, de otras no volátiles que se encuentran en la mezcla, como resinas o sales inorgánicas, u otros compuestos orgánicos no arrastrables.
OBJETIVO GENERAL
- El objetivo de la destilacion de un alcohol a vapor es separar una mezcla de varios componentes provechando sus distintas voltalidades.
MATERIALES
- 100ml de vino
- mechera
- termometro
- Matrax de fondo ovalado
- Manguera
- probeta
- Soporte universal
- Pinzas de soporte
- Alcohol etilico
- Tubo de esfero
PROCEDIMIENTO
- Se miden 100 ml de cerveza en la probeta.
- Luego se coloca en la matrax de fondo ovalado.
- Despues lo cerramos con un tapon
- Se prende el mechero con los 100ml de alcohol.
- Se conecta el tapon con una manguera , que permite su condensacion
- por ultimo medimos la temperatura con un termometro.
RESULTADO
CONCLUSION
Como conclusion decimos que todo el procedimiento fue exitoso y que nos dejo mucho conocimiento al momento de realizar este laboratorio practico y sencillo.
WEBGRAFIAS
- http://www.alambiques.com/destilaciones.htm
- https://es.m.wikipedia.org/wiki/Destilaci%C3%B3n
- https://es.slideshare.net/mobile/LuisMorillo2/practica-5-28304033















Es de mucha ayuda , esta información , gracias
ResponderEliminar